FDA设备和放射健康中心主任杰夫·舒伦(Jeff Shuren)博士说:“The Lucira COVID-19 & Flu Home Test的紧急授权是使消费者能更多地获得完全可以在家中自行诊断测试的一个重要里程碑。”
新冠、流感和呼吸道合胞病毒的叠加影响下,如何区分自己得的是哪种“感冒”?
当地时间2月24日,美国食品药物监督管理局(FDA)为首个可以区分新冠和流感的非处方(OTC)家庭诊断测试盒颁发了紧急使用授权(EUA)。
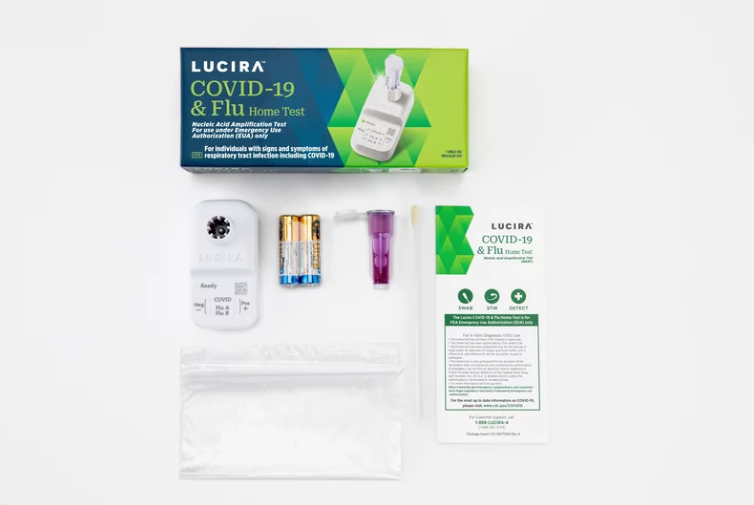
据悉,该测试盒名为The Lucira COVID-19 & Flu Home Test,是一种一次性的家庭测试盒,适用于具有呼吸道感染(包括COVID-19)症状的个人。由美国新冠检测试剂制造商Lucira Health开发。
该测试盒可以在没有处方的情况下购买并使用,14岁及以上的个人可自行收集鼻拭子样本,2岁及以上(14岁以下)的儿童可由成人为之采集,采集过程可完全在家中进行,30分钟内出结果,测试盒将显示个体在甲型流感、乙型流感和新冠三项中是阳性还是阴性。
FDA新闻稿称,在有症状的个体中,The Lucira COVID-19 & Flu Home Test正确识别了99.3%的阴性和90.1%的阳性甲型流感样本,100%的阴性和88.3%的阳性新冠样本以及99.9%的阴性乙型流感样本。由于目前没有足够的乙型流感病例纳入临床研究,EUA要求Lucira继续收集样本以研究该测试盒在现实世界中检测乙型流感的能力。FDA也提醒,与所有快速诊断测试一样,该测试盒也存在假阳性和假阴性结果的风险。
FDA设备和放射健康中心主任杰夫·舒伦(Jeff Shuren)博士说:“The Lucira COVID-19 & Flu Home Test的紧急授权是使消费者能更多地获得完全可以在家中自行诊断测试的一个重要里程碑。”
有趣的是,Lucira Health正是曾在2020年11月推出首个获得美国FDA批准的“新冠居家自检测试剂盒”的公司,称可在30分钟内提供“实验室质量的结果”。当地时间2月22日,Lucira Health宣布已根据美国破产法向美国特拉华州破产法院申请保护,破产期间,Lucira Health将继续经营支持客户需求,并寻求业务出售。
该公司CEO当时表示,新冠限制措施的下降抑制了对检测的需求,挤压了Lucira的利润,监管机构批准一款流感检测试剂盒的速度慢于预期也对公司造成了损害。
短短几天后,The Lucira COVID-19 & Flu Home Test获得FDA紧急使用授权。
